Bei gleichem Motorwirkungsgrad stößt Ethanol daher 4,56 / 3,55 = 1,28-mal mehr CO2 aus als Benzin, um die gleiche Aufgabe zu erfüllen.
Mit anderen Worten: Ethanol stößt 28% mehr CO2 aus als Benzin.
Und werden bei dieser Berechnung für Ethanol nicht berücksichtigt:
- CO2-Produktionskosten der Getreide- oder Zuckerfabrik
- Kosten für die Raffination der Pflanze zu Zucker
- Destillationskosten
- die Energiekosten der Fermentation (dh das CO2, das zum Erhitzen der Melasse freigesetzt wird)
Einige Erinnerungen an die Chemie: Zucker, Fermentation, Alkohol und CO2 ...
Wir werden die folgenden Atommassen beibehalten, die als Grundlage aller Berechnungen dienen: C = 12 g / mol, O = 16 g / mol, H = 1 g / mol
a) Der Fall von Alkohol aus der Fermentation von Zucker
Der zur Herstellung von Ethanol verwendete Zucker stammt aus der Familie von Diholoside (Saccharose oder Maltose) der Formel: C12H22O11 (siehe http://fr.wikipedia.org/wiki/Sucre#Chimie ) hat eine Molmasse von 342 Gramm, die durch Hydrolyse (es "gewinnt" ein Wassermolekül) 2 Moleküle Glucose oder 2 * C6H12O6 mit einer Molmasse von 180 Gramm für eine Gesamtmasse von 360 ergibt Gramm.
Glukosedetails: http://fr.wikipedia.org/wiki/Glucose
Das Mol Glucose wird dann gemäß der folgenden Gleichung fermentieren:
Code: wählen
C6H12O6 --> 2*C2H6O + 2*CO2Produkte: 2 Mol Ethylalkohol (C2H6O = 46 g / mol) und zwei Mol Kohlendioxid (CO2 = 44 g / mol).
Vor dem Verbrennen und Vernachlässigen anderer CO2-Emissionen wird daher bei der "Erzeugung" jedes Gramm produzierten Alkohols freigesetzt: 44/46 = 0.95 Gramm CO2.
Und das VOR seiner Verbrennung. Beim Verbrennen von Alkohol:
Code: wählen
C2H6O + 7/2*O2 --> 2*CO2 + 3*H2O oder für diejenigen, die runde Zahlen bevorzugen:
Code: wählen
2*C2H6O + 7*O2 --> 4*CO2 + 6*H20Ausgleichsfehler bei Reagenzien, Berichtigung (die die Ergebnisse bei CO2 nicht verändert):
Code: wählen
C2H6O + 3*O2 --> 2*CO2 + 3*H2O Beim Verbrennen erzeugt dieses Mol 46 g Alkohol daher 88 g CO2 (2 Mol).
Wir erhalten daher insgesamt 3 Mol CO2 pro Mol verbranntem Alkohol: 1 während der Fermentation und 2 während der Verbrennung. Insgesamt 3x44 = 132 g CO2 für 46 g verbrannten Alkohol.
Schlussfolgerung: Jedes Gramm Alkohol stößt daher bei seiner Herstellung und Verbrennung mindestens 132/46 = 2,87 Gramm CO2 aus.
Ich sage zumindest, weil viele "CO2-Positionen" nicht berücksichtigt wurden: Zuckerproduktion und Alkoholdestillation sind zweifellos die energiehungrigsten.
Dieser Wert von 2,87 g CO2 / g Alkohol ist daher ein sehr kleiner Wert!
b) Benzin (den Alkohol ersetzen soll)
Ich fahre fort, ohne die Berechnungen auf dieser Seite detailliert zu beschreiben: Verbrennungs- und CO2-Gleichungen
CO2-Emissionen für einen Kohlenwasserstoff der Formel C2H (2n + 2) = 44n
Anwendung auf Benzin (reine Oktan). n = 8
[C8H18] = 8 12 * + = 18 1 114 * g / mol.
Die pro verbrauchtem Mol Oktan freigesetzte CO2-Masse beträgt: 44 * 8 = 352 g.
Das Verhältnis von Kraftstoffverbrauch zu CO2-Emissionen beträgt 352/114 = 3,09
Schlussfolgerung: Jedes Gramm Benzin stößt daher bei seiner Verbrennung 3,09 Gramm CO2 aus
Die Kosten für das "Raffinieren" betragen im schlimmsten Fall 15%, man würde 3.55 g CO2 für das Raffinieren und die Verbrennung von Benzin erhalten.
c) Energievergleich Ethanol und Benzin
Code: wählen
PCI ethanol = 26 900 kJ/kg
PCI essence = 42 700 kJ/kg
Bei einem Motorwirkungsgrad sind daher 42,7 / 26,9 erforderlich = mal mehr Ethanolmasse, um die gleiche Energie bereitzustellen, dh das 1,59-fache.
In der Isoenergie Es ist daher notwendig, einen Koeffizienten von 1,59 für die CO2-Emissionen von Ethanol festzulegen: Die 2,87 Gramm werden daher zu 4,56 Gramm. Und denken Sie daran: Diese 2,87 g wurden bereits stark reduziert, weil sie den Zuckeranbau nicht berücksichtigten (aber Skeptiker werden mit gutem Grund sagen, dass wir für Benzin die Kosten von nicht berücksichtigt haben Rohextraktion und Transport)
Allgemeine Schlussfolgerung
Um die gleiche Menge an Verbrennungsenergie bereitzustellen, betragen die CO2-Emissionen jeweils:
- mit Benzin: 3,55 Gramm CO2
- mit Ethanol: 4,56 Gramm CO2
Bei gleichem Motorwirkungsgrad stößt Ethanol daher 4,56 / 3,55 = 1,28-mal mehr CO2 aus als Benzin, um die gleiche Aufgabe zu erfüllen.
Mit anderen Worten: Ethanol stößt 28% mehr CO2 aus als Benzin.
Und werden bei dieser Berechnung für Ethanol nicht berücksichtigt:
- CO2-Produktionskosten der Getreide- oder Zuckerfabrik
- Kosten für die Raffination der Pflanze zu Zucker
- Destillationskosten
- die Energiekosten der Fermentation (dh das CO2, das zum Erhitzen der Melasse freigesetzt wird)
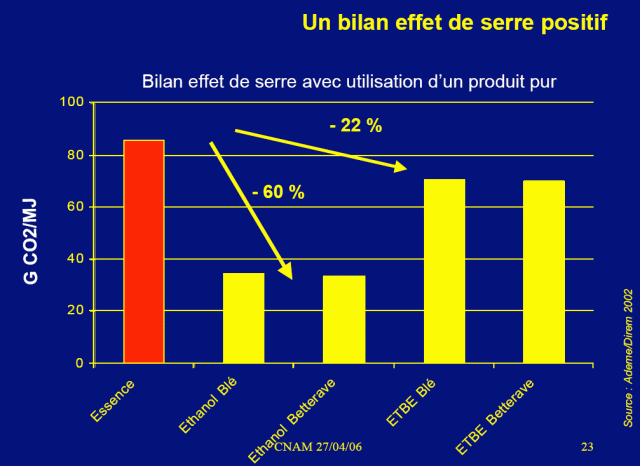
Es besteht daher kein Zweifel: Nach dieser Überlegung stößt Ethanol landwirtschaftlichen Ursprungs viel mehr CO2 aus als Benzin. Wie können staatliche Stellen und Universitäten solche positiven CO2-Berichte über Ethanol erhalten? Berücksichtigen sie nicht die Fermentation? Die Auslassungen sind sie? Oder wo liegt der Fehler in unserer Argumentation?